1.1.5 PET/SPECT:功能代谢
"功能成像让我们看到生命的活动,而不仅仅是身体的结构。" —— 医学影像学的新纪元
在前面的章节中,我们了解了CT、MRI和X射线这三种主要的解剖成像技术。现在,让我们进入发射断层成像的世界:PET 与 SPECT。它们不只回答“长什么样”,更试图回答“在做什么”——代谢、灌注、受体分布、炎症活性等。
🔬 第一部分:PET(正电子发射断层成像)
从反物质到医学影像
正电子的发现:反物质的第一次现身
1932年,美国物理学家卡尔·安德森(Carl Anderson)在加州理工学院研究宇宙射线时,在云室中观察到一种奇特的粒子轨迹:它的质量与电子相同,但电荷相反。这就是正电子(positron),人类发现的第一种反物质粒子。安德森因此获得1936年诺贝尔物理学奖。
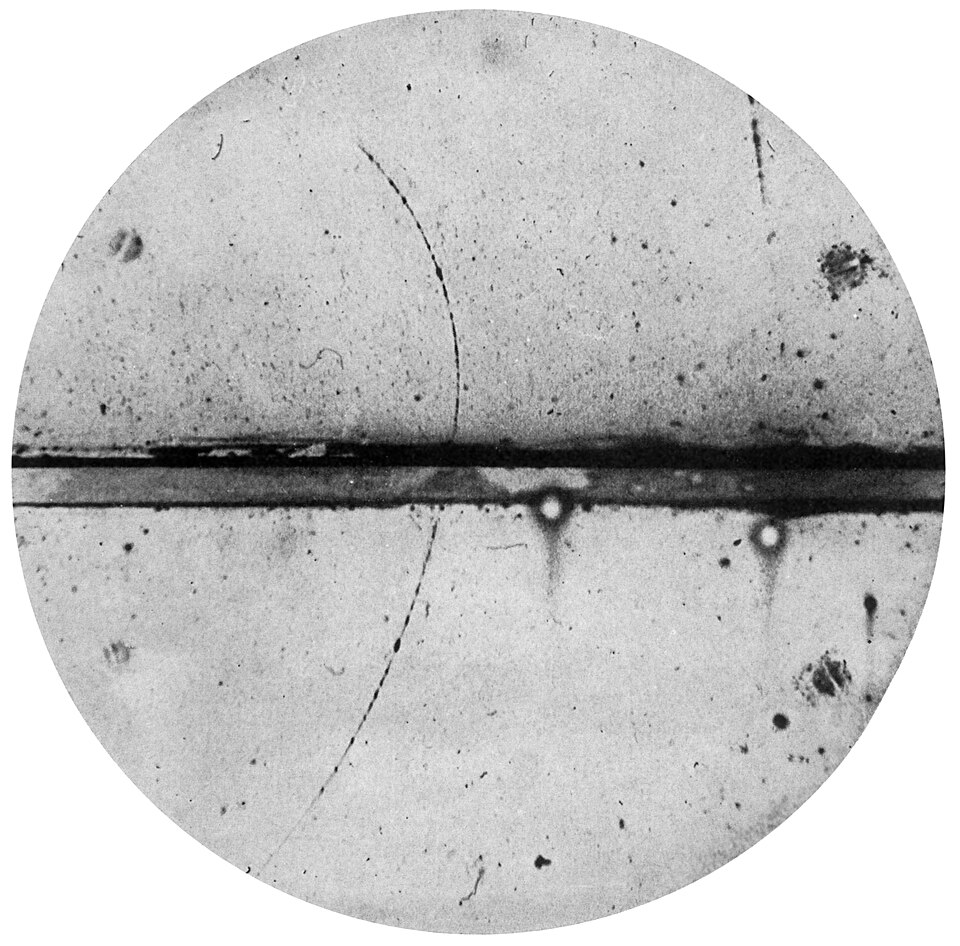 1932年安德森在云室中拍摄到的正电子轨迹照片,正电子从下方进入,穿过中间的铅板后弯曲更大(能量降低),证实了其正电荷特性
1932年安德森在云室中拍摄到的正电子轨迹照片,正电子从下方进入,穿过中间的铅板后弯曲更大(能量降低),证实了其正电荷特性
当时没有人想到,这个看似纯粹的物理学发现,会在几十年后彻底改变医学诊断。
💡 什么是反物质?
反物质是正常物质的"镜像":正电子是电子的反粒子,反质子是质子的反粒子。当物质与反物质相遇时,会发生湮灭(annihilation),质量完全转化为能量,产生高能光子。这个过程遵循爱因斯坦的质能方程 E=mc²。PET成像正是利用了这一物理现象。
放射性示踪剂:追踪生命的足迹
1943年,匈牙利化学家乔治·德·海韦西(George de Hevesy)因发展了放射性示踪剂技术而获得诺贝尔化学奖。他的开创性工作证明:可以用放射性同位素标记物质,然后追踪它们在生物体内的代谢过程。
这个想法为功能成像奠定了基础:如果我们能用放射性同位素标记葡萄糖,就能看到身体各部位的能量消耗情况。
首台PET扫描仪的诞生
1973年,在华盛顿大学医学院,物理学家迈克尔·菲尔普斯(Michael Phelps)和爱德华·霍夫曼(Edward Hoffman)在米歇尔·特尔-波戈相(Michel Ter-Pogossian)的指导下,制造出了世界上第一台PET扫描仪——PETT I(Positron Emission Transaxial Tomograph)。
这台设备只有一个探测环,扫描一次需要数小时,但它证明了PET成像的可行性。
FDG:PET成像的"燃料"
1976年,在美国布鲁克海文国家实验室,井户辰雄(Tatsuo Ido)、阿尔·沃尔夫(Al Wolf)和乔安娜·福勒(Joanna Fowler)成功合成了¹⁸F-氟代脱氧葡萄糖(FDG)。
FDG是葡萄糖的类似物,会被细胞摄取但不会被完全代谢,因此会在代谢活跃的组织中积聚。由于癌细胞的代谢速率通常是正常细胞的数倍,FDG-PET成为肿瘤诊断的利器。
🎯 为什么癌细胞"喜欢"葡萄糖?
这被称为瓦尔堡效应(Warburg effect):即使在有氧条件下,癌细胞也倾向于通过糖酵解获取能量,而不是更高效的有氧呼吸。这导致癌细胞对葡萄糖的摄取量远高于正常细胞,使得FDG-PET能够"点亮"肿瘤。
PET成像原理:捕捉湮灭的光芒
正电子湮灭:一场微观的"烟花"
PET成像的核心是正电子湮灭过程:
- 放射性示踪剂注射:将标记有正电子发射核素(如¹⁸F)的示踪剂(如FDG)注射到患者体内
- 正电子发射:放射性核素衰变,释放正电子
- 正电子湮灭:正电子在组织中行进很短距离(约1-2毫米)后,与电子相遇并湮灭
- 光子对产生:湮灭产生两个能量为511 keV的γ光子,以180度相反方向飞出
- 符合探测:PET扫描仪的探测器环同时探测到这对光子,确定湮灭发生的位置
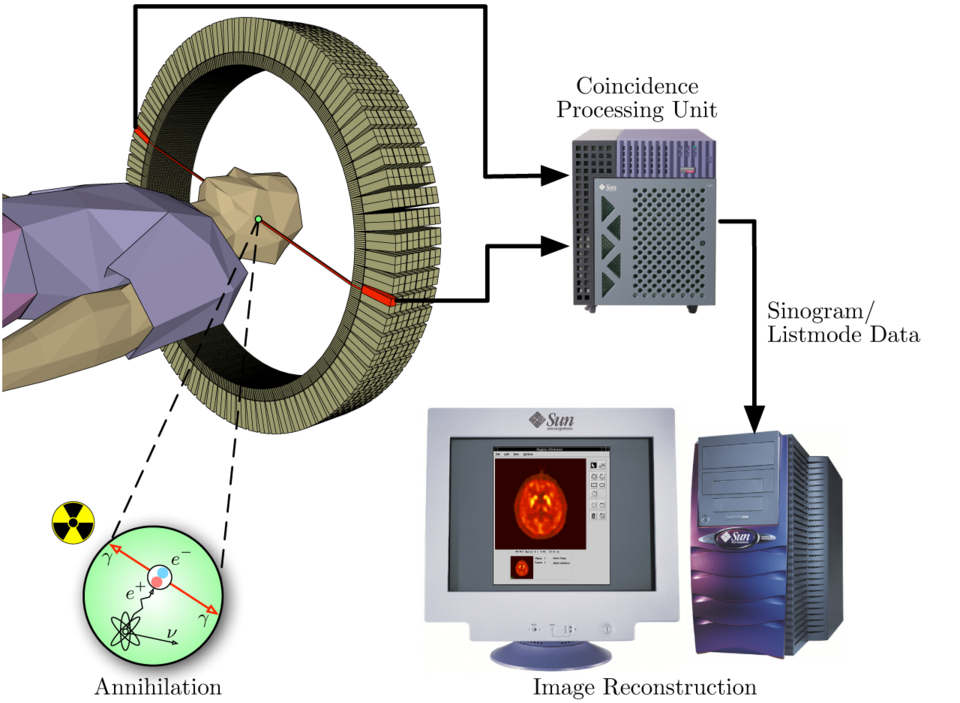 PET成像原理:正电子与电子湮灭产生两个方向相反的511 keV光子,被探测器环捕获,连线即为响应线(LOR)
PET成像原理:正电子与电子湮灭产生两个方向相反的511 keV光子,被探测器环捕获,连线即为响应线(LOR)
符合探测技术:时间就是一切
PET扫描仪使用符合探测(coincidence detection)技术:
- 只有在极短时间窗口内(通常<10纳秒)被两个相对的探测器同时探测到的光子对,才被认为来自同一次湮灭事件
- 这条连接两个探测器的直线称为响应线(Line of Response, LOR)
- 通过数百万条LOR的重建,可以得到示踪剂在体内的三维分布图像
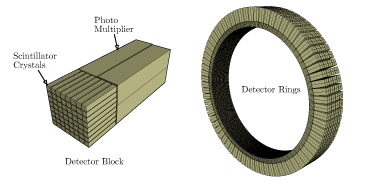 PET探测器系统结构:由闪烁晶体和光电倍增管组成的探测器块,排列成完整的探测器环
PET探测器系统结构:由闪烁晶体和光电倍增管组成的探测器块,排列成完整的探测器环
常用的放射性示踪剂
| 示踪剂 | 半衰期 | 标记核素 | 主要应用 |
|---|---|---|---|
| ¹⁸F-FDG | 110分钟 | ¹⁸F | 肿瘤、心脏、脑代谢 |
| ¹¹C-甲硫氨酸 | 20分钟 | ¹¹C | 脑肿瘤、蛋白质合成 |
| ¹³N-氨 | 10分钟 | ¹³N | 心肌灌注 |
| ¹⁵O-水 | 2分钟 | ¹⁵O | 脑血流 |
| ⁶⁸Ga-PSMA | 68分钟 | ⁶⁸Ga | 前列腺癌 |
⚠️ 放射性示踪剂的安全性
虽然PET使用放射性物质,但辐射剂量是可控的:
- 一次FDG-PET扫描的有效剂量约为5-7 mSv,相当于1-2次腹部CT
- 示踪剂的半衰期很短(¹⁸F为110分钟),会快速衰变
- 示踪剂用量极少(通常<10毫克),不会产生药理作用
- 孕妇和哺乳期妇女需要特别评估风险收益比
PET与CT/MRI的融合:1+1>2
单独的PET图像只显示功能信息,缺乏解剖细节。2000年,大卫·汤森(David Townsend)团队开发出第一台商用PET-CT扫描仪,被《时代》杂志评为"2000年度医学发明"。
PET-CT的优势:
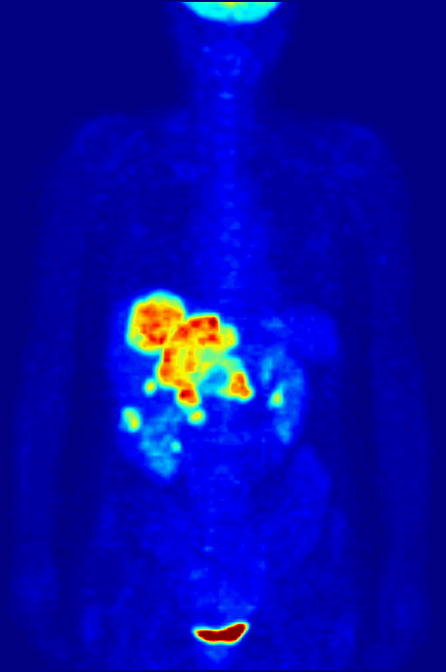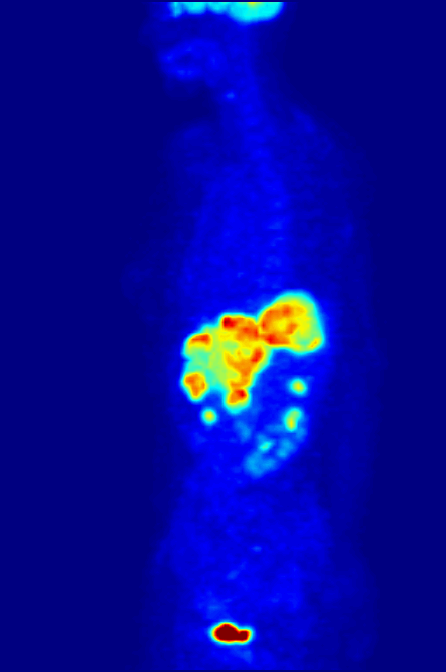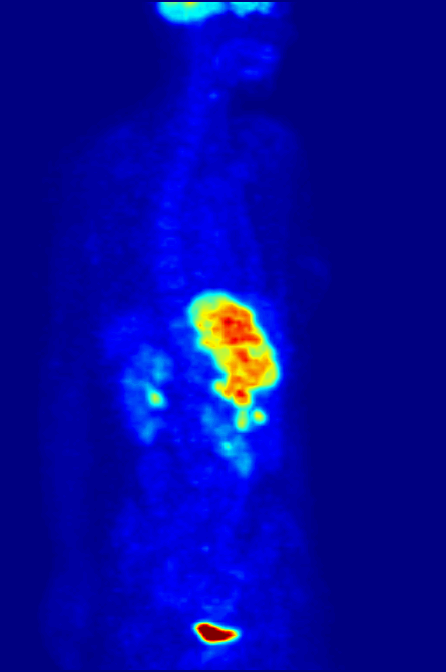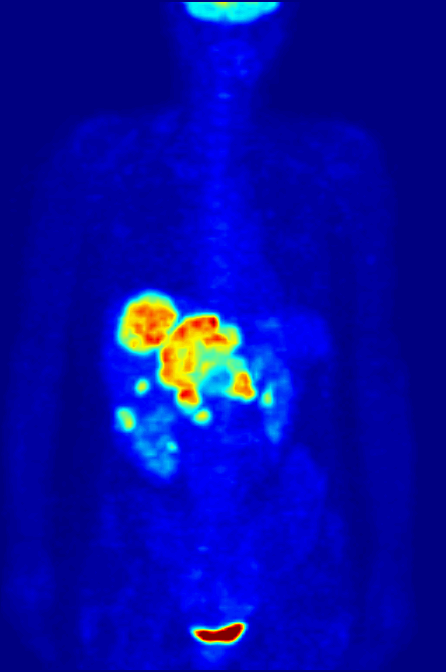 FDG-PET全身最大密度投影(MIP)扫描:正常脑部、肾脏和膀胱摄取FDG,肝脏可见异常高摄取灶提示转移
FDG-PET全身最大密度投影(MIP)扫描:正常脑部、肾脏和膀胱摄取FDG,肝脏可见异常高摄取灶提示转移
- CT提供精确的解剖定位
- CT数据用于PET图像的衰减校正,提高定量准确性
- 一次扫描同时获得功能和解剖信息
- 扫描时间从2小时缩短到30分钟
2010年代,PET-MRI开始应用于临床,结合了MRI的优秀软组织对比度和PET的功能成像能力,特别适合脑部和盆腔成像。
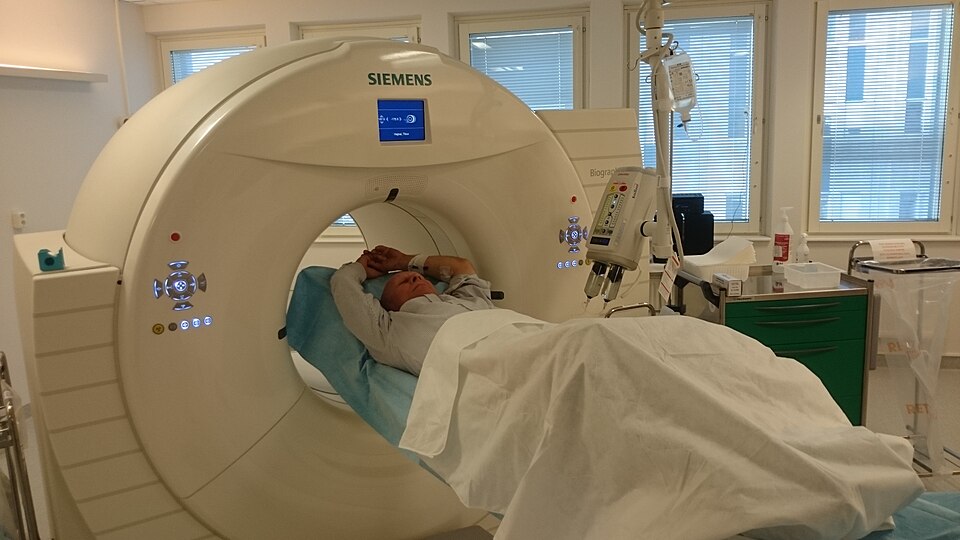 现代PET-CT扫描仪,将功能成像与解剖成像完美融合
现代PET-CT扫描仪,将功能成像与解剖成像完美融合
PET技术的发展历程
| 年代 | 里程碑事件 | 关键技术 | 扫描时间 | 主要应用 |
|---|---|---|---|---|
| 1970s-1980s | 概念验证阶段 | 单环探测器、BGO晶体 | 2-4小时 | 脑代谢研究 |
| 1973:首台PET扫描仪(PETT I) | ||||
| 1976:FDG合成成功 | ||||
| 1990s-2000s | 临床应用普及 | 多环探测器、全身扫描 | 30-60分钟 | 肿瘤诊断与分期 |
| FDG-PET成为肿瘤诊断标准 | ||||
| 1998:FDA批准FDG用于临床 | ||||
| 2000s | 融合成像时代 | PET-CT、LSO晶体 | 15-30分钟 | 肿瘤、心脏、神经 |
| 2000:首台商用PET-CT | ||||
| 时间飞行(TOF)技术 | ||||
| 2010s | 多模态与精准成像 | PET-MRI、数字PET | 10-20分钟 | 精准医学、早期诊断 |
| 2010:首台PET-MRI | ||||
| 全数字PET探测器 | ||||
| 2020s至今 | 全身与超快成像 | 全身PET、AI重建 | <10分钟 | 全身肿瘤筛查 |
| 长轴向视野(LAFOV)PET | ||||
| 超灵敏探测器 |
关键技术突破
| 技术类别 | 技术名称 | 时间 | 核心贡献 | 性能提升 |
|---|---|---|---|---|
| 探测器 | BGO晶体 | 1980s | 高密度、高阻止本领 | 提高探测效率 |
| 探测器 | LSO/LYSO晶体 | 2000s | 更快衰减时间 | 提高计数率、改善图像质量 |
| 探测器 | 数字SiPM | 2010s | 全数字化、高灵敏度 | 提高时间分辨率、降低剂量 |
| 成像技术 | 时间飞行(TOF) | 2000s | 利用光子到达时间差 | 提高信噪比30-40% |
| 成像技术 | 点扩散函数(PSF)重建 | 2000s | 补偿系统响应 | 提高空间分辨率 |
| 融合成像 | PET-CT | 2000 | 解剖+功能 | 提高诊断准确率、缩短扫描时间 |
| 融合成像 | PET-MRI | 2010 | 软组织对比+功能 | 减少辐射、提高软组织分辨率 |
| AI辅助 | 深度学习重建 | 2010s | 降噪、加速成像 | 降低剂量50%、缩短扫描时间 |
🚀 全身PET:一次扫描,全身尽览
2018年,加州大学戴维斯分校的研究团队开发出EXPLORER全身PET扫描仪,轴向视野长达2米,可以一次扫描覆盖全身。这种长轴向视野(LAFOV)PET的优势:
- 灵敏度提高40倍
- 扫描时间从20分钟缩短到1分钟
- 辐射剂量降低40%
- 可以进行全身动态成像,观察示踪剂在全身的实时分布
这为全身肿瘤筛查、系统性疾病诊断开辟了新的可能。
PET技术的临床意义
| 应用领域 | 典型应用 | 临床价值 | 常用示踪剂 |
|---|---|---|---|
| 肿瘤学 | 肿瘤诊断与分期 | 早期发现、准确分期、评估转移 | ¹⁸F-FDG |
| 疗效评估 | 早期判断治疗反应、调整方案 | ¹⁸F-FDG | |
| 放疗计划 | 精确定位肿瘤边界 | ¹⁸F-FDG、¹¹C-甲硫氨酸 | |
| 神经系统 | 阿尔茨海默病 | 早期诊断、鉴别诊断 | ¹⁸F-FDG、淀粉样蛋白示踪剂 |
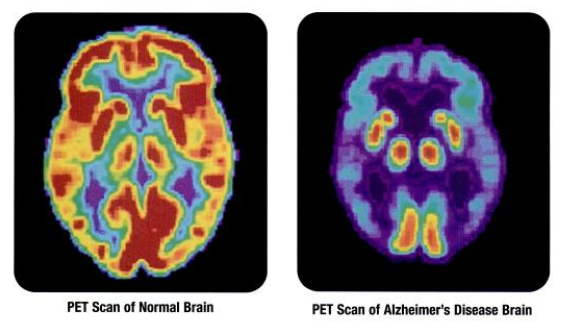 PET脑扫描对比:正常老年人(左)与阿尔茨海默病患者(右),患者脑部代谢活动明显减低
PET脑扫描对比:正常老年人(左)与阿尔茨海默病患者(右),患者脑部代谢活动明显减低
| | 癫痫 | 定位致痫灶 | ¹⁸F-FDG | | | 帕金森病 | 多巴胺系统评估 | ¹⁸F-DOPA | | 心血管 | 心肌活力评估 | 判断心肌是否可逆性损伤 | ¹⁸F-FDG、¹³N-氨 | | | 心肌灌注 | 评估冠状动脉疾病 | ¹³N-氨、⁸²Rb | | 感染/炎症 | 感染灶定位 | 不明原因发热的病因诊断 | ¹⁸F-FDG |
☢️ 第二部分:SPECT(单光子发射计算机断层成像)
如果说 PET 像是在捕捉“成对的湮灭光子”,那么 SPECT 则更像是在“收集单个γ光子的方向性信息”。它同样属于发射断层成像,但物理与系统实现有显著差异。
SPECT 的核心原理:单光子 + 准直器
SPECT 常用核素发射的是单个γ光子(例如 140 keV 的 Tc-99m)。难点在于:探测器接收到一个光子时,你并不知道它从哪里来。
为了解决“方向未知”的问题,SPECT 依赖关键部件:准直器(collimator)。
- 准直器由大量细小孔道组成,只允许满足几何方向的光子进入探测器
- 代价是:绝大多数光子会被吸收掉 → 灵敏度较低、采集时间较长
💡 为什么 SPECT 空间分辨率往往不如 PET?
PET 的符合探测天然给出一条 LOR(响应线),而 SPECT 需要靠准直器“筛方向”。准直器孔径越小,方向越准、分辨率越好,但灵敏度越低;孔径越大,灵敏度提高但分辨率变差——这是一个典型的系统折中。
SPECT 系统长什么样?
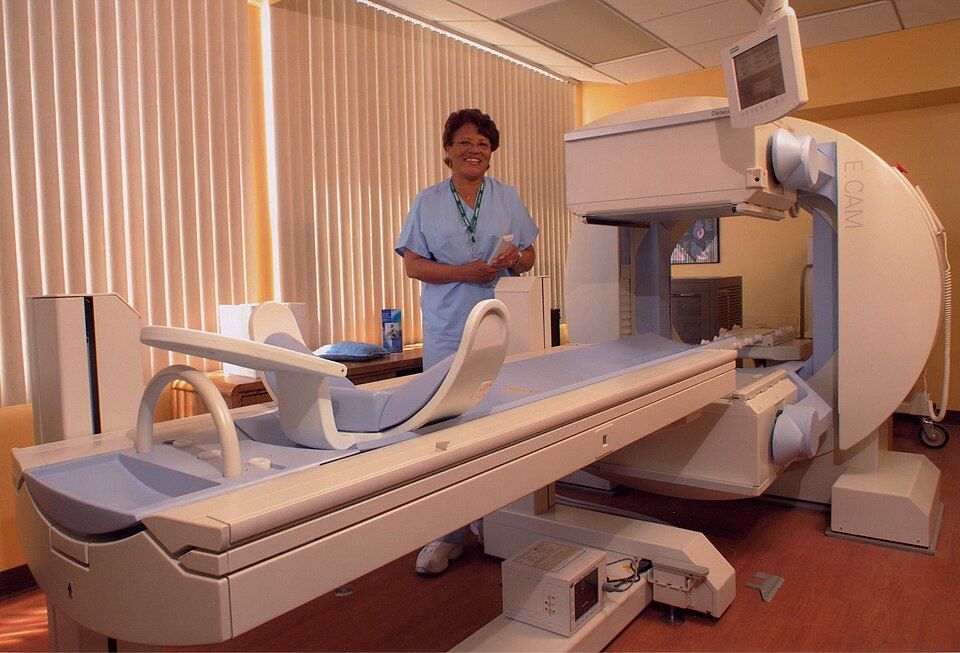 Siemens E.Cam SPECT伽马相机,探测器头可绕患者旋转采集多角度投影
Siemens E.Cam SPECT伽马相机,探测器头可绕患者旋转采集多角度投影
经典 SPECT 系统是γ相机(gamma camera) + 旋转采集:
- γ相机通常由闪烁晶体(如 NaI(Tl))、光电倍增管等组成
- 相机绕患者旋转,采集多角度投影(类似 CT 的“从不同角度拍照”)
- 之后通过重建算法获得 3D 放射性分布
随着多模态发展,临床常见 SPECT/CT:
- CT 用于解剖定位
- CT 也可用于 SPECT 的衰减校正(尤其对深部结构的定量更关键)
常用 SPECT 核素与示踪剂(示例)
| 核素/示踪剂(例) | 典型能量 | 半衰期(约) | 常见用途 |
|---|---|---|---|
| Tc-99m(MDP、MIBI 等) | 140 keV | 6 h | 骨显像、心肌灌注、甲状腺/肾功能等 |
| I-123 | 159 keV | 13 h | 甲状腺、神经递质相关检查 |
| Tl-201 | 70–80 keV(X射线) | 73 h | 心肌灌注(历史上常见) |
| In-111 | 171/245 keV | 67 h | 炎症/标记白细胞等 |
⚠️ 影像定量的“难点”
SPECT 的定量通常更“难”一些:能量更低、散射更明显,且准直器/系统响应更复杂,因此衰减校正、散射校正、系统响应建模对定量影响更大。
SPECT 的重建:从 FBP 到 OSEM
与 CT/PET 类似,SPECT 也经历了从解析到迭代的路径:
- FBP(滤波反投影):实现简单,但对噪声敏感,伪影较明显
- OSEM(有序子集期望最大化):更符合计数统计(泊松噪声),也更容易融合衰减/散射/系统响应模型,临床更常用
SPECT 的临床价值(为什么仍然重要)
 SPECT心肌灌注成像:评估冠状动脉供血情况,是心血管疾病诊断的重要工具
SPECT心肌灌注成像:评估冠状动脉供血情况,是心血管疾病诊断的重要工具
虽然 PET 发展迅速,但 SPECT 仍然非常重要,原因很现实:
- 可及性更高:不依赖回旋加速器(很多 SPECT 核素来源于发生器或供应链更成熟)
- 成本更低:设备与检查成本通常更友好
- 特定检查生态成熟:例如骨显像、部分心肌灌注方案等
🔍 PET vs SPECT:一张表说清楚
| 特性 | PET | SPECT |
|---|---|---|
| 探测对象 | 湮灭产生的成对 511 keV 光子 | 单个 γ 光子(能量随核素而异) |
| 方向信息来源 | 符合探测给出 LOR | 准直器提供方向选择 |
| 灵敏度 | 通常更高 | 通常更低(准直器损失大量光子) |
| 空间分辨率 | 通常更好(系统不同而不同) | 通常略差(与准直器强相关) |
| 定量能力 | 相对更成熟 | 也可定量,但对校正/建模更敏感 |
| 临床组合 | PET/CT、PET/MRI | SPECT/CT |
💡 关键要点总结
- PET 的本质:利用正电子湮灭产生的 511 keV 光子对,通过符合探测得到 LOR,再重建示踪剂分布。
- PET 的优势:灵敏度高、定量能力强,融合成像(PET/CT、PET/MRI)极大提升定位与临床价值。
- SPECT 的本质:单光子成像,通过准直器获得方向信息;系统响应与校正更复杂,但可及性与成本优势明显。
- 两者共性:都是"看功能"的发射断层成像;区别主要来自"光子如何被探测与定位"的物理机制。
📎 图片引用来源
- 正电子发现云室照片:Wikimedia Commons - PositronDiscovery,Public Domain
- PET成像原理示意图:Wikimedia Commons - PET-schema,Public Domain (Jens Maus)
- PET探测器系统:Wikimedia Commons - PET-detectorsystem,Public Domain (Jens Maus)
- FDG-PET全身扫描:Wikimedia Commons - PET-MIPS-anim,Public Domain (Jens Maus)
- PET脑扫描对比:Wikimedia Commons - PET scan normal brain vs Alzheimer's,Public Domain (NIA/NIH)
- SPECT伽马相机:Wikimedia Commons - Gamma camera,CC BY-SA 3.0
- SPECT心肌灌注成像:Wikimedia Commons - Heart spect imaging,CC BY 2.5 (Patrick J. Lynch)